引言:精准医学呼唤可控降解
蛋白水解靶向嵌合体(PROTAC)是一种能够同时结合E3泛素连接酶与疾病相关蛋白,并利用细胞内源性泛素-蛋白酶体系统降解靶蛋白的技术。然而,PROTAC的催化特性以及肿瘤的异质性可能带来不可控的蛋白降解、脱靶毒性以及无法精细调控的治疗窗口等问题,从而限制了其临床转化潜力。
基于此,可控型的PROTAC技术应运而生,其利用外界刺激或内部信号使降解活性在特定时间、特定地点或特定条件下被精确激活或关闭,实现对降解活性的时空调控。
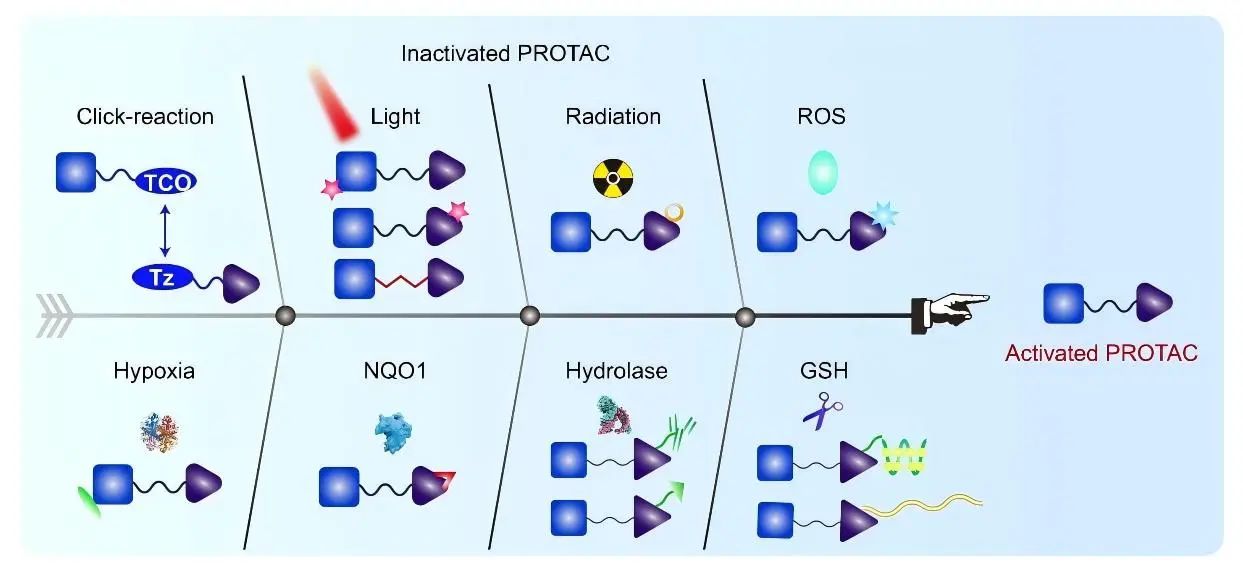
一、外界刺激/光控型PROTA
原理:利用光敏基团(光笼、光异构化基团)调控PROTAC活性。光照射前无活性/低活性,光照后释放活性分子或改变构象激活。
▲光裂解PROTAC(PC-PROTAC)
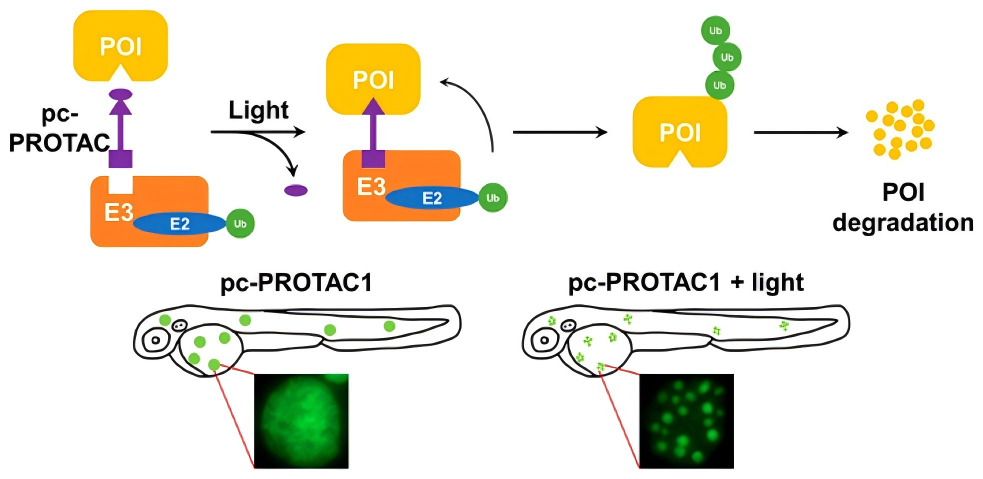
PC-PROTAC包含一个可光切割的光笼基团,可在特定光照射下释放活性 PROTAC,实现了"从无到有"的按需激活,避免脱靶毒性。2019年,Pan团队首次提出光笼式 PROTAC(PC-PROTACs)。该团队将DMNB光笼基团连接到 BRD4抑制剂JQ1的酰胺键的氮原子上设计得到了PC-PROTAC分子。所得分子 PC-PROTAC1 仅在365nm的紫外光照射后在活细胞中显示出有效的降解活性,有效地降解了斑马鱼中的BRD4 蛋白并产生预期表型变化。此外,该方法还被成功应用于构建靶向BTK的PC-PROTAC3。作为一种光诱导蛋白质降解的通用策略,其仍存在一定的局限性,如蛋白质降解的不可逆等;同时,需要紫外光的照射也限制了该技术在动物体内的安全应用。
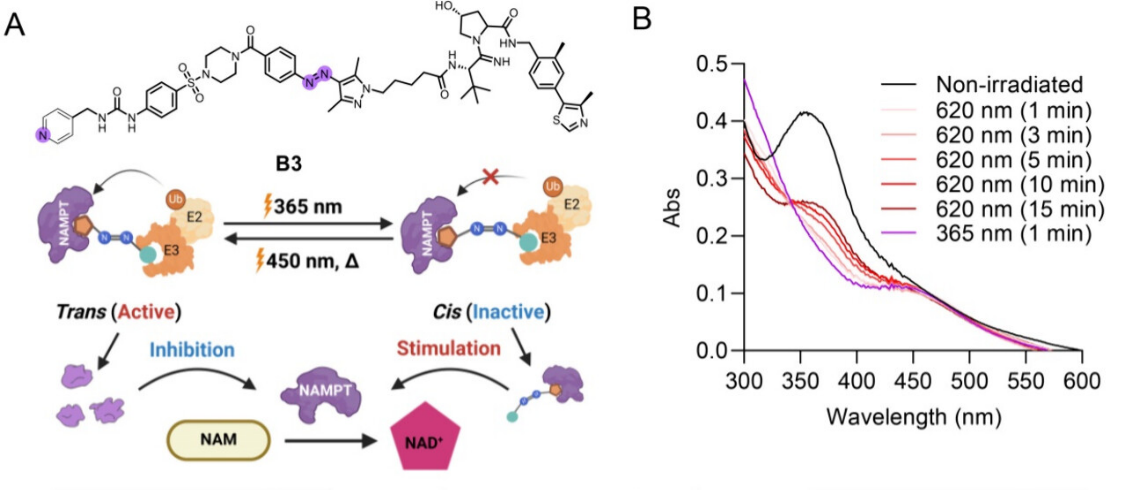
▲光开关PROTAC(PS-PROTAC)
与之类似,PS-PROTAC是在分子中嵌入光控异构单元(如偶氮苯或二芳基乙烯),其构型随光照可逆转换。光照下,由于Z/E构型转换而使连接子长度产生差异,从而可逆地改变靶蛋白配体与E3泛素连接酶配体间的距离,实现了蛋白降解的可逆调控。2024年,Sheng团队开发了一种新的 PS-PROTACs 设计策略。该研究以NAMPT激动剂作为靶蛋白配体,以具有高转化率和双稳态的光控元件二甲基吡唑偶氮苯作为连接子,设计合成了一类新型光控NAMPT PROTAC(PS-PROTAC)分子。该分子经450 nm光照后处于反式(E)构型,能够有效降解NAMPT,并下调细胞内NAD+;而经365 nm光照后处于顺式(Z)构型,对NAMPT无降解作用,发挥激动效应和上调细胞内NAD+。此外,通过增加光源功率和照射时间,620 nm波长同样能够促使PS-PROTAC进行Z/E构型的转换,从而实现小鼠体内移植瘤模型抗肿瘤活性、NAMPT和NAD+稳态调节的光学操控。
二、基于内部信号的智能响应型PROTAC
原理:利用疾病微环境(如肿瘤、炎症部位)特有的生物化学特征(酶、pH、ROS、GSH水平、缺氧等)来特异性激活PROTAC。
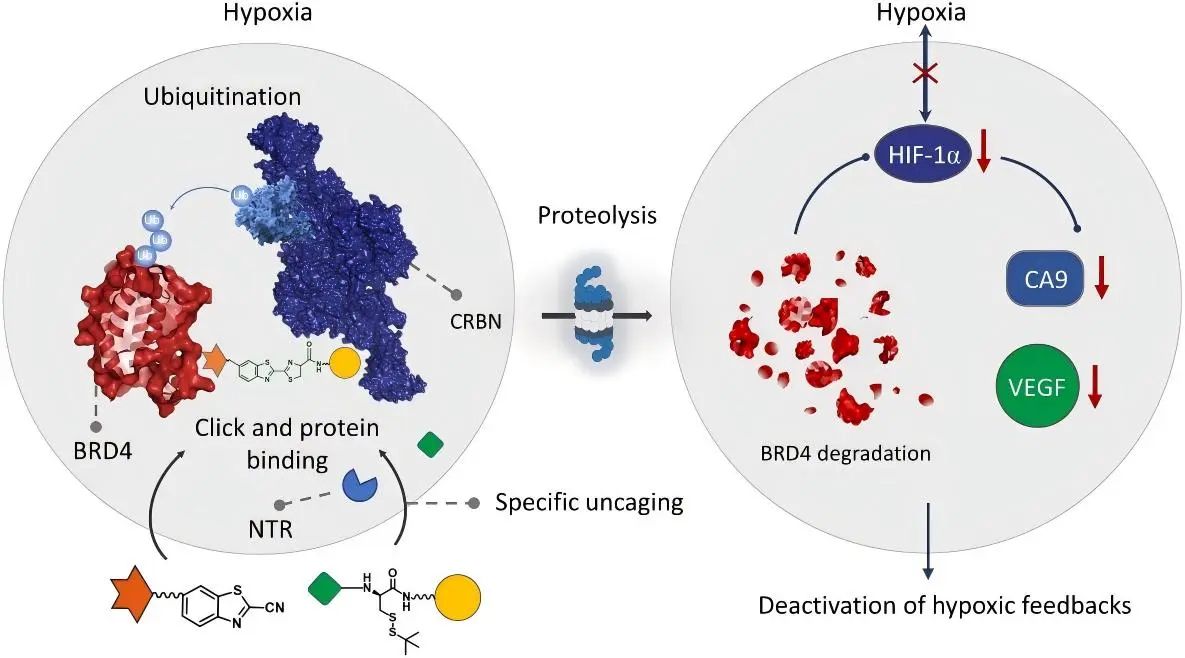
▲缺氧响应型PROTAC
缺氧是90%的实体瘤中广泛存在的一种特质,通常与肿瘤的增殖、分化、血管生成、能量代谢以及癌症的耐药性发生、患者预后较差密切相关。Xing等开发了一种点击式PROTAC(ENCTAC)系统,可用于低氧微环境中的刺激响应性蛋白质降解。该系统能够正交交联两个不同的小分子弹头配体,这些配体仅在缺氧诱导的硝基还原酶(NTR)激活后识别肿瘤内BRD4蛋白和E3连接酶。PROTAC分子的局部形成促进了BRD4的特异性下调,从而改变表观遗传靶标的表达,精确调节活细胞、斑马鱼和实体移植瘤模型的小鼠体内的缺氧信号传导。这一策略实现了选择性蛋白质降解,并且无需事先进行繁琐的化学合成。此外,这些小分子ENCTACs在体内表现出良好的药代动力学特征和有效的肿瘤抑制效果,有望为未来的精准医疗提供更加灵活和具有成药性的PROTAC干预手段。
▲酶响应型PROTAC
某些关键酶的异常表达是肿瘤和其他疾病的重要特征之一。肿瘤细胞不仅可以调节酶的经典功能来满足自身快速增殖的需要;同时还能调控多种复杂的细胞活动和疾病的发生发展过程。Zhang等设计了一种具有光疗和可控激活效力的PROTAC(SPNpro),用于光免疫代谢癌症的治疗。SPNpro可以远程生成单线态氧(1O2),根除肿瘤细胞,并诱导免疫原性细胞死亡(ICD)以增强肿瘤免疫原性。此外,SPNpro的PROTAC功能被癌症生物标志物(组织蛋白酶B)特异性激活,以触发活小鼠肿瘤中免疫抑制性吲哚胺2,3-双加氧酶(IDO)的靶向蛋白水解。持续的IDO降解可阻断肿瘤细胞中的色氨酸(Trp)代谢途径并促进效应T细胞的激活。研究结果表明,这种SPNpro介导的可激活光免疫代谢疗法增强了抗肿瘤T细胞免疫力,并有效抑制了肿瘤生长和转移。
结语:精准智控,破局前行
可控型PROTAC通过光、酶或小分子开关实现时空精准调控,显著降低脱靶毒性,显示了其在肿瘤靶向治疗中的应用前景。然而,该技术目前仍面临激活效率不稳定、调控元件可能破坏三元复合物稳定性及递送效率低等缺陷。为了促进可控型PROTAC 的临床应用,该技术未来发展需聚焦三大方向:
▲智能设计:优化外界刺激与内部信号的选择与结合,开发多元响应型PROTAC;
▲先进递送:结合纳米药物递送系统等方法实现口服给药及深层组织靶向递送;
▲临床转化:通过肿瘤等疾病模型验证推进临床转化,并探索与免疫疗法联用以克服耐药。
总之,通过与材料科学、纳米医学、生物正交化学等领域的融合,可控型PROTAC有望进一步丰富靶向蛋白降解的工具箱,加速迈向临床应用。
供稿:小分子药物实验室硕士研究生 陈晓彤
审核:朱成梁


